Изобар процесс
Изобар процесс нь даралт тогтмол үед явагддаг термодинамик процесс юм. Системд дулаан шилжүүлэхэд систем ажил хийх бөгөөд мөн системийн дотоод энерги өөрчлөгдөнө:
Термодинамикийн 1-р хуулийн дагуу энд W нь системийн хийсэн ажил, U нь дотоод энерги бөгөөд Q нь дулаан. Даралт эзэлхүүнээс хамаарсан ажилыг (системийн хийсэн) дараах байдлаар тодорхойлно: (Δ нь нийт процессын явцад гарсан өөрчлөлт гэсэн утгаар орсон бөгөөд дифференциал биш юм)
нэгэнт даралт тогтмол учир үүнийг ингэж бичиж болно
- .
Идеаль хийн тэгшитгэлийг орлуулбал
хийн хэмжээ тогтмол гэж үзвэл (тухайлбал химийн урвалын үед фазын өөрчлөлт гараагүй байж болно) ийм болно. Мөн
байдаг бөгөөд эдгээр сүүлийн хоёр тэгшитгэлүүдийг эхний тэгшитгэлд орлуулбал:
- .
хаалтан дотор буй хэмжигдэхүүн нь даралт тогтмол үеийн молийн дулаан бaгтаамж болно:
хэрэв изобар процесс явагдсан хий нь дан атомт хий бол and болно.
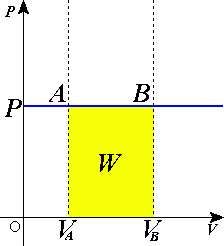
Изобар процессыг P-V диаграм дээр эхний термостатик төлөвөөс эцсийн төлөв хүртэл хөндлөн шулуун шугамаар харуулав. Хэрэв процесс баруун тийш шилжвэл энэ нь тэлэх процесс болох ба зүүн тийш шилжвэл агших процесс болно.
Энтальпиг тодорхойлох нь[засварлах | кодоор засварлах]
Изохор процессыг гэсэн тэгшитгэлээр тодорхойлдог. Изобар процессуудын хувьд мөн төсөөтэй тэгшитгэлийг гаргах нь зохимжтой. Хоёр дахь тэгшитгэлийг эхнийх орлуулбал
U + p V гэсэн хэмжигдэхүүн нь төлөвийн функц бөгөөд үүнийг энтальпи гэдэг ба H үсгээр товъёолдог. Тиймээс изобар процессыг илүү товч бөгөөд тодорхойгоор дараах байдлаар илэрхийлж болно:
- .














