Серин амин хүчил
| |||
| Нэр | |||
|---|---|---|---|
| IUPAC нэр
Serine
| |||
| Өөр нэр
2-Amino-3-hydroxypropanoic acid
| |||
| Ерөнхий | |||
| 56-45-1 (L-) 302-84-1 (DL-) 312-84-5 (D-) | |||
| ChEBI | CHEBI:17115 | ||
| ChEMBL | ChEMBL11298 | ||
| ChemSpider | 5736 (L-form) 597 | ||
| DrugBank | DB00133 | ||
| ЕХ дугаар | 206-130-6 | ||
| 726 | |||
| Jmol-3D зураг | Зураг Зураг | ||
| PubChem | 617 | ||
| UNII | 452VLY9402 (L-) 00PAR1C66F (DL-) 1K77H2Z9B1 (D-) | ||
| |||
| |||
| Шинж чанар | |||
| C3H7NO3 | |||
| Моль масс | 105.09 g·mol−1 | ||
| Гадаад байдал | white crystals or powder | ||
| Нягт | 1.603 g/cm3 (22 °C) | ||
| Хайлах температур | 246 °C (475 °F; 519 K) decomposes | ||
| soluble | |||
| Хүчиллэг (pKa) | 2.21 (carboxyl), 9.15 (amino)[1] | ||
Өөрөөр тодотгож заагаагүй бол бодисуудын хэвийн төлөв (25 °C [77 °F], 100 kPa) дахь үзүүлэлтүүд. | |||
| | |||
| Мэдээлэлийн хайрцагны эх сурвалж | |||
Серин (тэмдэглэгээ Ser эсвэл S) нь уургийн биосинтезд ашиглагддаг ɑ-амин хүчил юм. Энэ нь α-амин бүлэг (биологийн нөхцөлд үүсэх протонжуулсан −NH+
3 ), карбоксил бүлэг (физиологийн нөхцөлд протонгүй –COO−
), гидроксиметилийн бүлгээс бүрдэх хажуугийн гинжин хэлхээ, туйлын амин хүчил гэж ангилдаг. Энэ нь ердийн физиологийн нөхцөлд хүний биед нийлэгжиж, амин чухал хүчил үүсгэдэг. Үүнийг UCU, UCC, UCA, UCG, AGU, AGC кодлогчуудаар кодлодог.
Оршил
[засварлах | кодоор засварлах]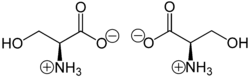
Энэхүү нэгдэл нь байгалийн гаралтай протеиноген амин хүчлүүдийн нэг юм. Зөвхөн L-стереоизомер нь уураг дотроос гардаг. Энэ нь хүний бие махбодид бусад метаболитууд, түүний дотор глицинээс нийлэгждэг тул хүний хоолонд зайлшгүй хэрэгтэй биш юм. Сериныг анх эх үүсвэр болох уургаас 1865 онд Эмил Крамер олж авсан. Нэр нь Латин хэлнээс торгон, серикум гэсэн үгнээс гаралтай. Серины бүтэц нь 1902 онд байгуулагдсан.
Биосинтез
[засварлах | кодоор засварлах]Серины биосинтез нь 3-фосфоглицератын исэлдэлтээс (гликолизоос завсрын) 3-фосфогидроксифират руу ба Фосфоглицератын дегидрогеназаар NADH(Никотинамид аденины динуклеотид) эхэлдэг . Энэхүү кетоныг фосфосферины трансаминазаар дахин хувиргах үйлчилгээ (фосфосин) нь фосфосферин фосфатазаар серин рүү гидролизддэг.
E. coli зэрэг бактериудад эдгээр ферментүүд сера (EC 1.1.1.95), serC (EC 2.6.1.52), serB (EC 3.1.3.3) генээр кодлогддог.

Глициний биосинтез: Серины гидроксиметилтрансфераза (SHMT = серийн траншидроксиметилаза) нь L-серины эргэлтийн хувирлыг глицин (ретро-алдолын задрал) ба 5,6,7,8-тетрофидрофолатыг 5,10-метиленететрахидрофолат (mTHF) болгон хувиргадаг .SHMT нь пиридоксаль фосфат (PLP) -аас хамааралтай фермент юм. Глицин нь CO2, NH4 +, mTHF-ээс глициний синтазаар урвалд орж урвалын үед үүсдэг.
Синтез ба үйлдвэрлэлийн бүтээмж
[засварлах | кодоор засварлах]Үйлдвэрлэлийн хувьд сериныг гидроксиметилтрансферазын катализ болох глицин ба метанолоос гаргаж авдаг.
Ракемийн сериныг лабораторид метил акрилатаас хэд хэдэн алхамаар бэлдэж болно :
Биологийн функц
[засварлах | кодоор засварлах]Метаболик
[засварлах | кодоор засварлах]
Серин нь метаболизмд чухал үүрэг гүйцэтгэдэг бөгөөд энэ нь пурин ба пиримидиний биосинтезд оролцдог. Энэ нь глицин, цистеин, бактери дахь триптофан зэрэг хэд хэдэн амин хүчлүүдийн анхдагч нөхцөл юм. Энэ нь биосинтезийн нэг нүүрстөрөгчийн хэлтэрхийн үндсэн тэтгэгч болох сфинголипид ба фолат зэрэг бусад олон метаболитүүдийн анхдагч нөхцөл юм.
Бүтцийн үүрэг
[засварлах | кодоор засварлах]Серин нь олон ферментүүдийн катализаторын үйл ажиллагаанд чухал үүрэг гүйцэтгэдэг. Энэ нь химитрипсин, трипсин болон бусад олон ферментүүдийн идэвхтэй газруудад тохиолддог болохыг харуулсан. Мэдрэлийн хийн гэгддэг бодис ба шавьж устгах үйлчилгээнд хэрэглэдэг олон бодис нь ферментийг бүрэн дарангуйлдаг ацетилхолины эфиразын идэвхтэй хэсэгт серины үлдэгдэлтэй нийлж үйл ажиллагаа явуулдаг болохыг харуулсан.
Серины хажуугийн гинжин хэлхээ нь ихэвчлэн устөрөгчтэй байдаг; Үүссэн хамгийн түгээмэл жижиг санаа нь ST эргэлт, ST хөдөлгөөнүүд (ихэвчлэн альфа хеликийн эхэнд байдаг) ба ST гол хэсгүүд (ихэвчлэн альфа хелүүдийн дунд байдаг).
Уургийн бүрэлдэхүүн хэсэг (үлдэгдэл) учраас түүний хажуугийн гинж нь O-гликозилизаци-ийг үүсгэдэг бөгөөд энэ нь чихрийн шижинтэй холбоотой байж болно.
Энэ нь эукариотуудад эсийн дохиоллын үед киназуудаар ихэвчлэн фосфоржуулсан гурван амин хүчлийн үлдэгдлийн нэг юм. Фосфоржуулсан серины үлдэгдлийг ихэвчлэн фосфосерин гэж нэрлэдэг.
Серины протеаз бол нийтлэг протеаз юм.
Дохио
[засварлах | кодоор засварлах]L-serine (түүний enantiomer) -аас үүссэн серемийн ракемазаар мэдрэлийн эсэд нийлэглэгдсэн D-Серин нь NMDA рецепторуудыг идэвхжүүлснээр нейромодуляторын үүрэг гүйцэтгэдэг бөгөөд дараа нь глутаматтай холбож өгдөг. D-Серин нь NMDA төрлийн глутамат рецепторын (NMDAR) гликиний талбайд хүчтэй агонист юм. Рецептор нээгдэхийн тулд глутамат ба глицин эсвэл D-серины аль алинд нь заавал холбогдох ёстой; үүнээс гадна нүх сүвийг хориглох ёсгүй (ж.нь Mg2 + эсвэл Zn2 +). Үнэндээ D-serine бол NMDAR (N-метил-D-аспартат)-ийн глициний талбай дээрх глицинээс илүү хүчтэй агонист юм.
D-serine нь саяханыг болтол зөвхөн бактерид байдаг гэж үздэг байсан; Энэ нь D-аспартатыг олсны дараахан тархинд дохионы молекул болох хүний биед байгалиас олж илрүүлсэн хоёр дахь D амин хүчил байв. Хэрэв хүний биед D амин хүчлийг эрт илрүүлэх байсан бол NMDA-ийн рецептор дээрх глициний хэсгийг D-серины хэсэг гэж нэрлэж болох юм. Төв мэдрэлийн системээс гадна D-serine нь мөгөөрс, бөөр, корпусын хөндий зэрэг захын эд, эрхтнүүдэд дохио өгдөг.
Амтны мэдрэмж
[засварлах | кодоор засварлах]L-Серин нь бага зэргийн умами бүхий чихэрлэг бөгөөд өндөр агууламжтай исгэлэн амттай байдаг.
Цэвэр D-серин нь маш бүдэг гичийн үнэртэй, цагаан өнгийн талст нунтаг юм. D-Серин нь дунд болон өндөр концентрацитай исгэлэн амттай байдаг.
Эмнэлзүйн ач холбогдол
[засварлах | кодоор засварлах]Серины дутагдлын эмгэг нь амин хүчил L-серины биосинтезийн ховор согог юм. Одоогийн байдлаар 3 эмгэг фосфоглицератын дегидрогеназын дутагдал, 3-фосфосферины фосфатазын дутагдал, фосфосфрин аминотрансферазын дутагдалтай байна. Эдгээр ферментийн гажиг нь төрөлхийн микроцефали ба сэтгэлзүйн хүнд хэлбэрийн хомсдол гэх мэт мэдрэлийн хүнд шинж тэмдгүүдэд хүргэдэг ба 3-фосфоглицератын дегидрогеназын дутагдалтай өвчтөнүүдэд хураан авахад хүргэдэг. Эдгээр шинж тэмдгүүд нь L-serine, заримдаа глицинтэй хавсарч эмчлэхэд янз бүрийн түвшинд хариу үйлдэл үзүүлдэг. Эмчилгээний хариу арга хэмжээ нь хувьсах шинж чанартай бөгөөд урт хугацааны болон үйл ажиллагааны үр дүн нь тодорхойгүй байна. Эдгээр өвчний тархвар судлал, генотип / фенотип хоорондын хамаарал, үр дагаврын талаархи ойлголтыг сайжруулж, өвчтөний амьдралын чанарт нөлөөлөх, оношлогоо, эмчилгээний стратегийг үнэлэх зорилгоор өвчтөний бүртгэлтэй олон улсын арилжааны бус байгууллага байгуулжээ. Нейротрансмиттертэй холбоотой эмгэгүүд.
Эмчилгээний зориулалтаар ашиглах судалгаа
[засварлах | кодоор засварлах]L-Серин-ийг амин чухал хүчил гэж ангилах нь нөхцөлт гэж тооцогддог тул сээр нуруутан амьтдад хүмүүс бүхэл бүтэн амьдралын туршид оновчтой хэмжээг нэгтгэж чаддаггүй. Шизофрени, L-сериныг эмчлэх боломжтой тул D-Serine-ийг мэрэгч амьтдын дунд судалж байгаа бөгөөд FDA-ийн батлагдсан хүний клиник туршилтанд Амиотрофийн хажуугийн склероз эмчлэх боломжтой. 2011 оны мета-анализд сөрөг ба нийт шинж тэмдгүүдэд дунд зэргийн нөлөө үзүүлдэг саркозиныг илрүүлсэн. D-Серин нь магадгүй Альцгеймерийн өвчний(AD) эрт үеийн оношлогоо (AD) -ийг оношлох боломжтой биомаркер гэж тодорхойлсон байна. Учир нь магадлалтай AD өвчтнүүдийн тархины нугасны шингэн дэх харьцангуй өндөр агууламжтай байдаг. L ‐ серины эмчилгээг олж авах боломжтой гэсэн нотолгоо байдаг.
Ном зүй
[засварлах | кодоор засварлах]- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. p. C-512. ISBN 0-8493-0462-8.
{{cite book}}: Unknown parameter|name-list-format=ignored (|name-list-style=suggested) (help)